Sepsis ist nicht nur eine Blutvergiftung – Sepsis ist eine lebensbedrohliche Erkrankung mit hohen Todesraten. Eine schnelle und verlässliche Diagnose der verursachenden Erreger ist von entscheidender Bedeutung für das Überleben erkrankter Personen; etwas, das der momentane klinische Standard nicht umfassend erfüllt. Neue biointelligente Tests und Methoden, basierend auf geeigneten Biomarkern, können Patientinnen und Patienten bessere Überlebenschancen ermöglichen. Zum zweiten Teil dieser Blog-Serie reisen wir in den Blutkreislauf und geben Sepsis-Erregern keine Chance.
Im ersten Teil dieser Blog-Serie haben wir Biomarker etwas genauer unter die Lupe genommen, also Moleküle mit prognostischer/diagnostischer Aussagekraft für einen biologischen oder krankhaften Prozess. Wir von der In-vitro-Diagnostik am Fraunhofer IGB nutzen zellfreie DNA (cfDNA). Doch wie machen wir das und was ist nochmal Sepsis?
Sepsis – ein unterschätztes Problem?
Ein Patient wird aufgrund einer Entzündung im Bauchraum mit Verdacht auf Sepsis in die Intensivstation verlegt. Jetzt müssen Ärzte schnell handeln und die korrekte medikamentöse Therapie verabreichen. Jedoch kann innerhalb kurzer Zeit kein Erreger detektiert werden; es müssen Breitbandantibiotika gegeben werden, um einen Großteil der potenziellen Erreger bekämpfen zu können. Dies basiert jedoch rein auf Vermutungen und der Zustand des Patienten verschlechtert sich lebensbedrohlich. Die medikamentöse Therapie scheint nicht zu wirken, möglicherweise sind es die falschen Antibiotika? Die Uhr tickt, während das Patientenleben auf der Kippe steht. Um Patient*innen korrekt und schnell behandeln zu können, müssen die verursachenden Erreger diagnostiziert werden. Dies kann jedoch mehrere Tage dauern und lässt Mediziner*innen im Dunkeln tappen.
Doch was ist überhaupt Sepsis? Das Wort Sepsis stammt aus dem Griechischen und bedeutet übersetzt Zersetzung oder Zerfall. Die medizinische Behandlung hat sich in den vergangenen Jahrzehnten stetig verbessert, dennoch bleibt Sepsis eine lebensbedrohliche Erkrankung, verbunden mit hohen ökonomischen und sozialen Belastungen. Jährlich erkranken rund 280.000 Menschen in Deutschland an Sepsis mit Todesraten von 25 bis 40 Prozent. Weltweit entfallen ca. 20 Prozent der jährlichen Todesfälle auf eine Sepsis-Erkrankung (Stand 2017). Grundlage einer Sepsis sind Infektionen mit Mikroorganismen; meistens Bakterien, aber ebenso können Viren, Pilze oder Parasiten auslösend sein. Gerade bei langen Krankenhausaufenthalten steigt die Gefahr einer Infektion zum Beispiel im Atemtrakt, an offenen Wunden oder an Kathetern. Einem besonderen Risiko sind vor allem Menschen mit Prädispositionen ausgesetzt, wie chronischen Erkrankungen, Diabetes, Übergewicht oder Immunschwäche. Gerade ältere Menschen sind deswegen besonders anfällig für schwere Verläufe. Dies führt erst zu unspezifischen Symptomen wie erhöhten Entzündungsparametern, flacher Atmung oder Fieber, später dann aber bis hin zu Organversagen. Das Immunsystem gerät außer Kontrolle, produziert vermehrt entzündungsfördernde Stoffe und richtet damit zusätzlich Schäden an. Deswegen ist eine schnelle und korrekte Behandlung der Sepsis notwendig. Je früher spezifisch behandelt werden kann, desto effektiver. Neben der symptomatischen Behandlung zur Kreislaufstabilisation werden Antiinfektiva wie Antibiotika verabreicht, um die verursachenden Pathogene zu bekämpfen. Hier stoßen wir jedoch auf ein Problem: die Erregerdiagnostik.
Wenn die Diagnostik mehr Fragezeichen als Antworten gibt…
Zur Pathogenbestimmung wird eine Blutkulturanalyse eingesetzt. Hierbei wird Blut abgenommen und auf verschiedenen Nährböden zur Identifikation des oder der Erreger kultiviert. Diese Nachweismethode ist zwar kostengünstig und schonend, bringt jedoch auch Nachteile mit sich. So kann es einige Tage dauern, bis Bakterien angewachsen sind – und dies kostet wertvolle Zeit, um Patient*innen spezifische Behandlungen und damit bessere Überlebenschancen zu ermöglichen. Zusätzlich können nicht alle Erreger durch diese Methode identifiziert werden, Kontaminationen und Behandlungen das Ergebnis verfälschen. In vielen Fällen kann das Ergebnis der Blutkultur negativ sein, obwohl eine Sepsis zugrunde liegt. Nur 10 bis 30 Prozent der Blutkulturanalysen sind laut Literatur positiv und korrekt. Und hier schließt sich der Kreis: Die Sepsis-Forschung ist auf der Suche nach neuen diagnostischen Methoden – mit biointelligenten Biomarkern zur schnellen, verlässlichen Detektion verursachender Erreger.
Wie tragen wir zur verbesserten Sepsis-Diagnostik bei?
Wir von der In-vitro-Diagnostik am Fraunhofer IGB nutzen cfDNA als unseren Biomarker der Wahl, welche von normalen Körperzellen, aber auch Sepsis-Erregern ins Blut abgegeben wird. Mittels der in Teil 1 beschrieben Liquid Biopsy entnehmen wir Patient*innen eine geringe Menge Blut und isolieren daraus die cfDNA. Doch wie geht es damit weiter?
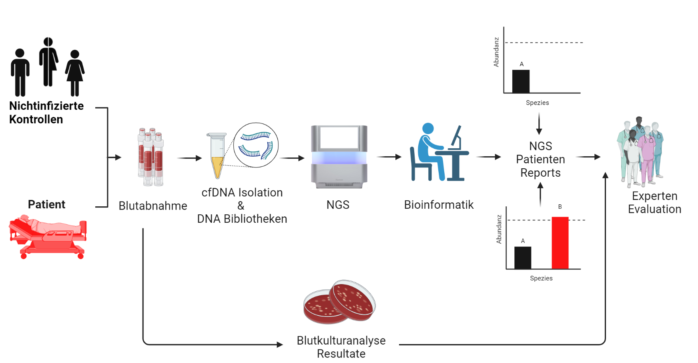
Die Theorie dahinter basiert auf einer Kombination aus molekularbiologischen Methoden und anschließender bioinformatischer Verarbeitung. Wie in Abbildung 1 zu sehen, wird die cfDNA nach erfolgter Isolation aus Plasma unter sterilen Bedingungen zu DNA-Bibliotheken weiterverarbeitet. Durch die Generierung dieser Bibliotheken ist eine anschließende Sequenzierung mittels Next-Generation Sequencing (NGS) möglich. Die erhaltene Menge an sequenzierter Information, sogenannte Reads, wird bioinformatisch weiterverarbeitet, gefiltert und normalisiert: Nach erfolgter Qualitätskontrolle werden alle humanen Reads, also die vom Patienten selbst stammenden Informationen, verworfen. Die verbliebenen Reads werden nun mit einer spezifisch dafür entwickelten Datenbank verglichen, welche die Genome von Bakterien, Viren, Pilzen und anderen Erregern enthält. Durch das Vergleichen der Reads mit den Sequenzen in der Datenbank können die Erreger identifiziert werden. Mit dieser bioinformatischen Analyse wird ein sogenannter SIQ Score (»sepsis indicating quantifier«) für jedes identifizierte Pathogen ermittelt. Dieser wird für jeden Erreger mit nichtinfizierten Kontrollpersonen verglichen, um Kontaminationen zu erkennen. Sofern der ermittelten SIQ-Score einen Schwellenwert überschreitet, werden die betreffenden Patient*innen als SIQ-positiv für dieses Pathogen diagnostiziert (Grumaz et al. 2016). Die in diesen Experimenten erhaltenen Ergebnisse waren sehr vielversprechend und so wurde eine monozentrische klinische Studie von 48 Sepsis-Patient*innen zusammen mit dem Uniklinikum Heidelberg gestartet, in der dieser Ansatz mit dem in Kliniken weit verbreiteten, diagnostischen Standard der Blutkulturanalyse verglichen und von Expert*innen evaluiert wurde. In dieser klinischen Studie konnte laut überwältigender Expertenmehrheit gezeigt werden, dass die NGS-getriebene Sequenzierung von cfDNA zur Sepsis-Diagnostik der Blutkulturanalyse deutlich überlegen ist: So wurde mittels Blutkulturanalyse in nur 11 Prozent der Patient*innen ein verursachendes Pathogen nachgewiesen, wohingegen durch die NGS-Diagnostik bei 71 Prozent der Patient*innen ein oder mehrere Pathogene identifiziert wurden. Darüber hinaus schätzten die klinischen Expert*innen in 96 Prozent der SIQ-positiven Ergebnisse diese auch als plausibel ein, was in 53 Prozent der Fälle zu einer veränderten und adäquateren Therapie geführt hätte (Grumaz et al. 2019).
Um diese vielversprechenden Ergebnisse weiter zu validieren, wurde eine 500 Sepsis-Patient*innen und 17 Kliniken umspannende, multizentrische klinische Studie gestartet (Brenner et al. 2018). Die Daten hierzu sind noch nicht veröffentlicht, aber es zeigt sich bereits in der Auswertung, dass die vorherigen Ergebnisse in puncto Sensitivität, Spezifität und Plausibilität bestätigt werden.
»Die Zukunft kann man am besten voraussagen, wenn man sie selbst gestaltet«
Dieses Zitat des Informatik-Pioniers Alan Kay gilt gerade im Bereich der zukunftsorientierten, biointelligenten Gesundheitsdiagnostik. Die NGS-basierte Analyse von Sepsis-Erregern aus cfDNA steht mittlerweile Kliniken durch eine Ausgründung aus unserem Institut zur Verfügung und kann helfen, durch eine exakte Pathogenbestimmung und daraus folgender präziser Therapie das Leben von Patient*innen zu retten. Wir bleiben hier jedoch nicht stehen – in Zukunft steht eine klinische Studie zur Sepsis bei Neugeborenen und Frühchen an, die ebenfalls sehr gefährdet sind. Zusätzlich entwickeln wir unter anderem neue, schnellere und kostengünstigere Methoden zur Diagnostik bei Sepsis-Patient*innen. Doch das ist eine Geschichte für einen weiteren Teil dieser Blog Serie – bis zum nächsten Mal, wenn es wieder heißt: Auf den Spuren von Sherlock Holmes: Wenn Forschende zu Detektiven werden.
Interesse geweckt?
Das Innovationsfeld In-vitro-Diagnostik steht für die Etablierung, Entwicklung und Verwertung diagnostischer Verfahren für biologische und medizinische Anwendungsgebiete. Dabei werden innovative Verfahren der Molekularbiologie, Biochemie und der Bioinformatik entwickelt, kombiniert und angewendet. Durch unsere jahrelangen Erfahrungen im Bereich der Erregerdiagnostik bei Sepsis besitzen wir eine weitreichende Expertise auf diesem Themengebiet und wollen diese stetig in anderen Bereichen wie zum Beispiel der Pankreaskrebsdiagnostik weiterentwickeln. Die Next-Generation-Sequencing-Technologie (NGS) zur Hochdurchsatzsequenzierung von Nukleinsäuren stellt dabei eine der zentralen Technologieplattformen innerhalb des Innovationsfelds dar. So nutzen wir NGS auch für die De-novo-Sequenzierung von Bakterien und Pilzen, Transkriptionsprofilanalysen, die Identifizierung relevanter Gene oder in der Corona-Diagnostik. Wenn Sie mehr darüber erfahren möchten, dann treten Sie gerne mit uns im Kontakt. #WeKnowHow
Links:
NGS-basierte Diagnostik von Krankheitserregern bei Sepsis
Weiterführende Literatur
Grumaz S, Stevens P, Grumaz C, Decker SO, Weigand MA, Hofer S, Brenner T, von Haeseler A, Sohn K. Next-generation sequencing diagnostics of bacteremia in septic patients. Genome Med. 2016 Jul 1;8(1):73.
Grumaz S, Grumaz C, Vainshtein Y, Stevens P, Glanz K, Decker SO, Hofer S, Weigand MA, Brenner T, Sohn K. Enhanced Performance of Next-Generation Sequencing Diagnostics Compared With Standard of Care Microbiological Diagnostics in Patients Suffering From Septic Shock. Crit Care Med. 2019 May;47(5)
Brenner T, Decker SO, Grumaz S, Stevens P, Bruckner T, Schmoch T, Pletz MW, Bracht H, Hofer S, Marx G, Weigand MA, Sohn K; TIFOnet Critical Care Trials Group. Next-generation sequencing diagnostics of bacteremia in sepsis (Next GeneSiS-Trial): Study protocol of a prospective, observational, noninterventional, multicenter, clinical trial. Medicine (Baltimore). 2018 Feb;97(6)

